Perguntas e respostas com Paul Nghiem, MD, PhD

A Skin Cancer Foundation conversou com Paul Nghiem, MD, PhD, sobre o progresso histórico na detecção, monitoramento e tratamento de pacientes com carcinoma de células de Merkel (MCC), um câncer de pele raro, mas perigoso. Dr. Nghiem (pronuncia-se NEE-em) é o George F. Odland Endowed Chair e chefe de Dermatologia da Universidade de Washington em Seattle. Ele é um dos maiores especialistas em MCC nos EUA
Perguntas e respostas
P: O melanoma mata mais pessoas do que qualquer outra forma de câncer de pele. Mas enquanto o carcinoma de células de Merkel (MCC) é muito mais raro do que o melanoma, é mais perigoso caso a caso. O que o torna mais perigoso?
R: Os primeiros MCCs são tipicamente muito menos evidentes do que os melanomas iniciais. Eles não parecem preocupantes, então muitas vezes acabam sendo detectados em um estágio mais avançado, quando metastatizam (espalham) para outras partes do corpo e são mais difíceis de curar. Em contraste, muitos melanomas são realmente encontrados no estágio in situ (estágio 0), quando estão contidos na camada mais superficial da pele (epiderme) e não invadiram as camadas mais profundas. Esses melanomas in situ são fáceis de tratar e praticamente não têm chance de metástase. Mas dos mais de 1,000 casos de MCC que estamos acompanhando, tivemos apenas duas lesões in situ. É muito raro detectá-los tão cedo.
Quando você encontra pela primeira vez um melanoma ou tumor MCC, a preocupação inicial é se as células tumorais podem ter metástase da lesão (o tumor primário) para os gânglios linfáticos mais próximos. A maneira padrão de verificar isso hoje é o biópsia do linfonodo sentinela (SLNB). Neste teste, o médico verifica se nenhuma célula cancerígena se espalhou para os gânglios linfáticos, removendo e examinando microscopicamente os primeiros gânglios próximos que recebem a drenagem do fluido linfático do tumor primário. Com o melanoma, na maioria dos casos, o tumor é pequeno e está em um estágio inicial o suficiente para que você não precise fazer um SLNB, pois é muito improvável que tenha metástase. No entanto, mesmo o menor MCC, com apenas quatro ou cinco milímetros de diâmetro, tem 15% de chance de se espalhar para os gânglios linfáticos ou além, então consideramos fazer um SLNB mesmo que um MCC seja muito pequeno.
P: O que as pessoas podem fazer para descobrir mais dessas lesões quando elas são facilmente curáveis? Como eles podem reconhecer potenciais MCCs mais cedo?
R: Os sinais clássicos de melanoma do ABCDE não funcionam para o carcinoma de células de Merkel. Em vez disso, temos o acrônimo, A E I O U, que pode ajudar no reconhecimento precoce: Asintomático/ausência de sensibilidade; Eexpandindo-se rapidamente; Isupressão imune; Ocom mais de 50 anos; e Upele clara/exposta a ultravioleta. Cerca de 63 por cento dos pacientes MCC têm lesões em rápida expansão, e cerca de 90 por cento têm três ou mais das características AEIOU. É importante observar, no entanto, que muitas lesões com várias das características AEIOU não provam ser MCC - algumas são benignas e outras podem ser um câncer de pele diferente.
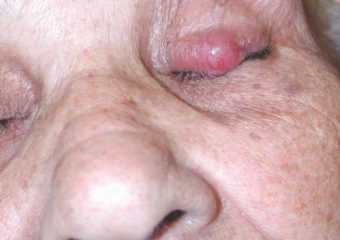
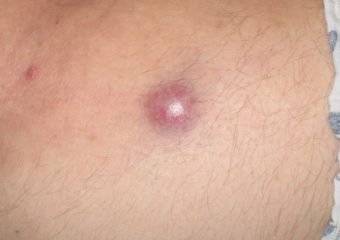
Fotos cortesia de Paul Nghiem, MD, PhD
P: Uma vez que um MCC tenha metástase para os gânglios linfáticos ou além, quais são as chances de sobrevivência do paciente?
R: É difícil dizer agora, porque graças aos novos tratamentos, a sobrevida está mudando rapidamente para melhor. Eu costumava me sentir sem esperança se alguém desenvolvesse MCC metastático, mas agora claramente não há esperança. Houve grandes mudanças na área, com possibilidade real de cura ou quase cura para o CCM avançado. Agora sinto que pelo menos metade dos pacientes com MCC metastático serão efetivamente tratados.
P: Que tratamentos fizeram a diferença?
R: No passado, tratávamos o carcinoma avançado de células de Merkel com quimioterapia. Essa abordagem reduziria os tumores em mais da metade dos casos, mas o benefício duraria apenas três meses em média. Quando o câncer voltou, era resistente a muitas drogas, e o sistema imunológico havia sido suprimido pela quimioterapia, agravando os problemas para o que é um câncer muito sensível ao sistema imunológico. No entanto, os inibidores de ponto de verificação são uma nova classe empolgante de imunoterapias (tratamentos que aumentam a capacidade do sistema imunológico de combater uma doença) e se tornaram o padrão de tratamento para MCC avançado. Ao bloquear os receptores de proteínas que normalmente mantêm o sistema imunológico sob controle, essas drogas estimulam as células T a combater o tumor.
Em março de 2017, a Food and Drug Administration (FDA) dos EUA aprovou um medicamento imunoestimulante, o avelumab (Bavencio), para o tratamento de adultos e pacientes pediátricos com 12 anos ou mais com MCC metastático. A aprovação da FDA, a primeira para MCC avançado, foi baseada em dados de um ensaio clínico em que 33 por cento dos pacientes experimentaram encolhimento completo ou parcial de seus tumores, embora todos tenham recebido quimioterapia anteriormente para seu MCC. Estudos subsequentes de avelumabe mostraram taxas de resposta mais altas quando administrado como terapia de “primeira linha” (antes da quimioterapia), com cerca de 50% dos pacientes se beneficiando.
Injetado por via intravenosa, o avelumabe estimula as células T bloqueando uma molécula chamada PD-L1 (ligante de morte programado 1) que se liga ao PD-1 para inibir essas células imunes críticas.
Em 2018, o FDA aprovou o pembrolizumab (Keytruda) para o tratamento de MCC, após um estudo de pacientes com MCC localmente avançado ou metastático recorrente que não receberam anterior terapia sistêmica para a doença mostrou 56 por cento objetivo taxa de resposta (ORR).
Em 2023, FDA concedeu aprovação acelerada para retifanlimabe-dlwr, também um PD-1 inibidor, como um tratamento para adultos com avanço local metastático ou recorrented MCC. éafety e eficácia foram baseadas em dados do estudo POD1UM-201 que avaliou o tratamento em adultos com MCC metastático ou localmente avançado recorrente que não receberam terapia sistêmica anterior para a doença. Esses pacientes apresentaram uma ORR de 52 por cento.
Eu costumava me sentir sem esperança para pacientes com MCC metastático. Agora, claramente não é impossível.
P: Existe alguma ordem preferencial na qual os tratamentos devem ser administrados agora? Você tem que administrar quimioterapia ou radiação primeiro, antes de usar uma das terapias de bloqueio de checkpoint?
R: Até recentemente, a quimioterapia era a terapia de primeira linha. Mas se você tratar MCC avançado com um inibidor de checkpoint antes de fazer quimioterapia, cerca de 60 por cento dos pacientes respondem. Se você esperar até que o paciente tenha falhado em uma rodada de quimioterapia, parece que cerca de 40 por cento dos pacientes respondem. E após duas ou mais rodadas de quimioterapia, cerca de 20 por cento dos pacientes respondem. Portanto, geralmente a abordagem correta agora parece ser usar primeiro a droga imunoestimulante e depois decidir o que fazer a seguir com base na resposta. Alguns pacientes terão uma resposta completa, com remissão total da doença. Os tumores de alguns pacientes responderão parcialmente, muitas vezes diminuindo em 70 por cento no volume do tumor, o que ainda é uma resposta importante. Muitos desses pacientes acabam tendo um baixo nível de doença que não afeta em nada sua saúde. Uma mulher que tratei recentemente teve uma resposta parcial por um ano, depois mudou para uma resposta completa. Mas geralmente, se o medicamento vai funcionar, a resposta vem rapidamente (dentro de 1-2 meses), e a maioria das respostas dura mais de um ano. No entanto, não temos certeza do que acontecerá quando o medicamento for interrompido.
Como o avelumabe agora é aprovado pela FDA para MCC que foi ou não previamente tratado com quimioterapia, ele agora está sendo usado preferencialmente como terapia de primeira linha para MCC metastático, enquanto a quimioterapia não é favorecida na maioria dos casos. Os dados atuais sugerem que a imunoterapia funciona melhor se administrada antes da quimioterapia, que tende a suprimir o sistema imunológico e tornar os tumores mais resistentes a uma variedade de tratamentos.
Embora a quimioterapia não seja mais o tratamento de linha de frente usual, a radiação pode, em alguns casos, ser usada com vantagem no início do jogo. Pode sinergizar muito bem com a imunoterapia. O sistema imunológico é melhor na eliminação de pequenos tumores do que de grandes tumores, e a radiação pode efetivamente encolher os tumores. Se a resposta à imunoterapia não for completa, lesões individuais que não respondem às vezes podem ser tratadas com um pouco de radioterapia para facilitar o trabalho do sistema imunológico.
P: E as outras terapias de bloqueio de checkpoint aprovadas pela FDA para melanoma, nivolumab (Opdivo®) e combinação de ipilimumab (Yervoy®)-nivolumab? Eles também estão sendo julgados pelo MCC?
R: Há uma quantidade crescente de dados disponíveis sobre como a combinação 'ipi-nivo' funciona na MCC. Sua principal aplicação tem sido para pacientes que não respondem a um único agente imunoestimulante (avelumabe ou pembrolizumabe). Para tais pacientes 'refratários', parece que a combinação ipi-nivo pode ajudar em cerca de 20 a –30 por cento dos casos. Em contraste, o ipi-nivo geralmente não é usado inicialmente porque a taxa de resposta aproximada de ~ 60 por cento para pembrolizumabe ou avelumabe sozinho é bastante alta, e a inclusão de ipilimumabe (Yervoy) na terapia imunológica é bem conhecida por adicionar efeitos colaterais significativos em comparação com um único PD -1 medicamento de via (como avelumabe ou pembrolizumabe).
P: O que acontece a seguir se nenhuma das terapias iniciais funcionar?
R: Esta é uma grande área de interesse e pesquisa. Conforme observado acima, a combinação 'ipi-nivo' pode ajudar em cerca de 20 a -30% dos casos de MCC que não respondem a uma única terapia de ponto de controle imunológico. Também é possível que injeções locais de terapias imunoestimulantes possam ser combinadas com um agente sistêmico, como a imunoterapia. Outras abordagens que estão sendo exploradas incluem dar aos pacientes células T assassinas específicas do câncer geneticamente otimizadas, semelhantes às células 'CAR-T' que se mostraram benéficas para certos tipos de câncer no sangue.
P: Você disse que espera que cerca de metade dos pacientes se saiam bem com as terapias de bloqueio de checkpoint. Isso sugere que cerca de metade não. Como esses são tratamentos caros com alguns efeitos colaterais potencialmente graves, há alguma maneira de saber com antecedência quais pacientes se beneficiarão, para que você possa iniciar os não respondedores previstos com um tratamento mais benéfico?
R: Embora mais da metade dos pacientes respondam, para cerca de 40 por cento dos pacientes, o câncer continua progredindo como se você não estivesse dando nenhum tratamento. Nós e muitos outros estamos trabalhando arduamente para resolver esse problema, e tenho o prazer de dizer que há progresso nessa área após mais de cinco anos de trabalho. Parece que os pacientes que têm um bom número de células T específicas do câncer no sangue são muito mais propensos a responder aos inibidores de checkpoint do que aqueles que não têm. Fascinantemente, o número de células T específicas do câncer nos tumores não prediz a resposta. Para usar uma analogia de batalha militar, parece que o número de tropas efetivas disponíveis como reforços (no sangue) é crítico para vencer a guerra. Em contraste, o número que encontramos no campo de batalha (no tumor), não é importante. Essas descobertas sugerem que, se pudermos aumentar o número de células T específicas do câncer disponíveis para o paciente, poderemos ajudá-las a combater melhor o câncer.
P: E depois de um curso de tratamento ter sido administrado? Existe uma maneira de saber desde o início se o câncer está começando a voltar?
R: Fizemos avanços empolgantes nessa área. Nossa equipe desenvolveu um exame de sangue, que procura certos anticorpos do poliomavírus das células de Merkel no sangue, para que possamos detectar quaisquer recorrências precocemente, quando o tumor será tratável com mais eficácia (consulte www.merkelcell.org/sero).
Em 2008, Patrick S. Moore, MD e Yuan Chang, MD descobriram que a maioria dos carcinomas de células de Merkel é parcialmente causada por um vírus. (A luz solar também costuma desempenhar um papel importante.) Encontramos esse poliomavírus de células de Merkel em cerca de 80% dos tumores MCC. Quando esse vírus infecta as células, ele produz oncoproteínas (proteínas promotoras do câncer) que podem fazer com que as células cresçam fora de controle. Fazemos o exame de sangue em intervalos diferentes, começando no momento do diagnóstico, e se o número de anticorpos dessas proteínas do poliomavírus aumentar, isso indica fortemente que o paciente está tendo uma recidiva.
Agora estamos usando esse teste rotineiramente, porque é muito útil no tratamento de pacientes ao longo do tempo. Cerca de metade dos pacientes não produz nenhum desses anticorpos e, na verdade, eles correm um risco cerca de 40% maior de recorrência do MCC do que aqueles que produzem os anticorpos; portanto, sabemos que precisamos acompanhá-los de perto com outras abordagens. Para os pacientes que produzem os anticorpos é relativamente simples: se o câncer não voltar, os anticorpos caem rapidamente e, na maioria dos casos, são indetectáveis um ano após o tratamento. Se o MCC voltar, os anticorpos aumentam. Isso nos dá uma grande chance de descobrir recorrências precocemente, quando elas são extremamente tratáveis: tratar uma uva em vez de uma toranja (em termos de tamanho do câncer) faz uma grande diferença. E com um paciente cujos anticorpos continuam caindo, o exame de sangue nos dá grande confiança de que o câncer não está recorrente, então podemos pular ou reduzir o uso de exames de imagem caros.
A partir de 2022, estamos envolvidos no desenvolvimento de outro teste que detecta pedaços de DNA do câncer que estão flutuando no sangue. Isso é chamado de teste de 'DNA tumoral circulante'. Tem sido usado para cânceres, incluindo mama e cólon. Parece funcionar particularmente bem para o MCC. Uma grande vantagem desse teste é que ele funciona mesmo em pacientes que não produzem anticorpos para o vírus Merkel. Portanto, praticamente todos os pacientes com MCC devem fazer um exame de sangue que normalmente é mais preciso e sensível do que os exames corporais
P: Depois de ter tratado pacientes com MCC, como você decide com que frequência vê-los e quanto risco eles ainda têm de o câncer voltar?
R: Em abril de 2022 recentemente relatamos que o risco geral de recorrência do MCC é de 40%; esta é uma taxa significativamente mais alta do que os cânceres de pele mais comuns. Além disso, está claro que o estágio do câncer de um paciente na apresentação e outros fatores de risco afetam muito seu próprio risco de recorrência de CCM. Esses fatores incluem supressão imunológica, sexo masculino e idade avançada, todos os quais aumentam o risco de recorrência. Dado que 95 por cento das recorrências ocorrem nos primeiros três anos após o diagnóstico, o tempo desde o diagnóstico é um fator muito importante que determina a chance restante de um paciente de que seu MCC ainda repita. Isso, por sua vez, é muito útil para determinar com que agressividade os pacientes devem ser acompanhados.
Criamos uma 'calculadora de risco' baseada na web. que leva em consideração esses vários fatores. Está disponível através www.merkelcell.org/recur.
Em nossa prática diária, isso provou ser incrivelmente útil. Por exemplo, quando os pacientes o procuram para a consulta de acompanhamento de um ano, agora é possível dizer a eles quanto risco “residual” de doença eles têm, em comparação com a chance assim que a vigilância começou.
Em geral, agora acreditamos que não precisamos monitorar os pacientes tão de perto por tantos anos como costumávamos fazer. MCC não parece ser como o melanoma, que muitas vezes recorre cinco ou 10 anos após o diagnóstico. Com o MCC, se ele voltar, geralmente ocorre dentro de dois a três anos. Então, agora pensamos que o acompanhamento intensivo por dois ou três anos é geralmente apropriado, com um cronograma marcadamente menos agressivo até o quinto ano.
P: Alguma outra nova forma de tratamento está fazendo diferença?
R: As imunoterapias de bloqueio de ponto de verificação mudaram o jogo, e nenhuma outra terapia sendo testada fez esse tipo de diferença ainda. No entanto, em combinação com a terapia de checkpoint, agora estamos usando células T dos próprios pacientes para combater o câncer. Em alguns casos, “reprogramamos” as células do paciente para atacar o câncer ao reconhecer o vírus. Em outros casos, encontramos e expandimos suas próprias células T específicas do vírus Merkel. Isso pode dar um impulso ao sistema imunológico, e combinar essa terapia com a terapia de bloqueio de ponto de verificação pode ser mais eficaz do que qualquer uma das abordagens isoladamente.
Também estamos procurando combinar algumas terapias intralesionais com as terapias de bloqueio de checkpoint. Em pequenos estudos em MCC, eles frequentemente encolheram ou eliminaram os tumores injetados e reduziram alguns outros tumores em todo o corpo. Estudos estão em andamento, mas parece provável que alguns desses estimuladores imunológicos “locais” administrados junto com agentes de ponto de controle imunológico ajudem a produzir taxas de resposta mais altas do que os agentes de ponto de controle administrados sozinhos.
Publicado em 7 de novembro de 2016. Atualizado em 21 de setembro de 2022.
