Fragen und Antworten mit Paul Nghiem, MD, PhD

Die Skin Cancer Foundation sprach mit Paul Nghiem, MD, PhD, über bahnbrechende Fortschritte bei der Erkennung, Überwachung und Behandlung von Patienten mit Merkelzellkarzinom (MCC), einem seltenen, aber gefährlichen Hautkrebs. Dr. Nghiem (ausgesprochen NEE-em) ist der George-F.-Odland-Stiftungslehrstuhl und Leiter der Dermatologie an der University of Washington in Seattle. Er ist einer der führenden Experten für MCC in den USA
Fragen und Antworten
F: An Melanomen sterben mehr Menschen als an jeder anderen Form von Hautkrebs. Das Merkelzellkarzinom (MCC) ist zwar viel seltener als das Melanom, aber von Fall zu Fall gefährlicher. Was macht es gefährlicher?
A: Frühe MCCs sind typischerweise weit weniger auffällig als frühe Melanome. Sie sehen nicht besorgniserregend aus, daher werden sie oft in einem fortgeschritteneren Stadium entdeckt, wenn sie Metastasen gebildet (sich ausgebreitet) haben und schwerer zu heilen sind. Im Gegensatz dazu werden viele Melanome tatsächlich im In-situ-Stadium (Stadium 0) gefunden, wenn sie in der obersten Hautschicht (Epidermis) enthalten sind und nicht in die tieferen Schichten eingedrungen sind. Diese In-situ-Melanome sind einfach zu behandeln und haben praktisch keine Chance auf Metastasierung. Aber von mehr als 1,000 MCC-Fällen, die wir verfolgen, hatten wir nur zwei In-situ-Läsionen. Es ist sehr selten, sie zu einem so frühen Zeitpunkt zu entdecken.
Wenn Sie zum ersten Mal ein Melanom oder einen MCC-Tumor finden, besteht die erste Sorge darin, ob Tumorzellen möglicherweise von der Läsion (dem Primärtumor) zu den nächstgelegenen Lymphknoten metastasiert haben. Die Standardmethode, dies heute zu überprüfen, ist die Sentinel-Node-Biopsie (SLNB). Bei diesem Test überprüft der Arzt, dass sich keine Krebszellen in die Lymphknoten ausgebreitet haben, indem er die ersten paar nahe gelegenen Knoten entfernt und mikroskopisch untersucht, die Lymphflüssigkeit aus dem Primärtumor erhalten. Beim Melanom ist der Tumor in den meisten Fällen klein und befindet sich in einem frühen Stadium, sodass Sie keine SLNB durchführen müssen, da es sehr unwahrscheinlich ist, dass er Metastasen gebildet hat. Allerdings hat selbst das kleinste MCC mit einem Durchmesser von nur vier oder fünf Millimetern eine 15-prozentige Wahrscheinlichkeit, dass es sich auf die Lymphknoten oder darüber hinaus ausgebreitet hat. Daher ziehen wir die Durchführung eines SLNB in Betracht, selbst wenn ein MCC sehr klein ist.
F: Was können Menschen tun, um mehr dieser Läsionen zu entdecken, wenn sie leicht heilbar sind? Wie können sie potenzielle MCCs früher erkennen?
A: Die klassischen ABCDE-Zeichen des Melanoms funktionieren beim Merkelzellkarzinom nicht. Stattdessen haben wir das Akronym AEIOU, die bei der Früherkennung helfen können: Asymptomatisch/mangelnde Empfindlichkeit; Eschnell expandieren; IImmununterdrückung; Oälter als 50 Jahre; und UUV-exponierte/helle Haut. Etwa 63 Prozent der MCC-Patienten haben sich schnell ausdehnende Läsionen und fast 90 Prozent weisen drei oder mehr der AEIOU-Merkmale auf. Es ist jedoch wichtig zu beachten, dass sich viele Läsionen mit mehreren der AEIOU-Merkmale nicht als MCC erweisen – einige sind gutartig und andere können ein anderer Hautkrebs sein.
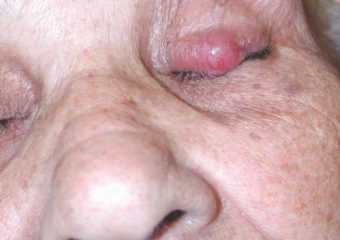
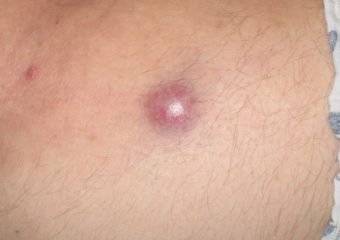
Fotos mit freundlicher Genehmigung von Paul Nghiem, MD, PhD
F: Wie sind die Überlebenschancen des Patienten, wenn ein MCC in die Lymphknoten oder darüber hinaus metastasiert ist?
A: Das ist im Moment schwer zu sagen, denn dank neuer Behandlungen verändert sich das Überleben schnell zum Besseren. Früher fühlte ich mich hoffnungslos, wenn jemand metastasierendes MCC entwickelte, aber jetzt ist es eindeutig nicht hoffnungslos. Es gab große Veränderungen auf diesem Gebiet, mit einer echten Heilungs- oder Fast-Heilungsmöglichkeit für fortgeschrittenes MCC. Ich habe jetzt das Gefühl, dass mindestens die Hälfte der Patienten mit metastasiertem MCC effektiv behandelt werden wird.
F: Welche Behandlungen haben den Unterschied gemacht?
A: In der Vergangenheit haben wir das fortgeschrittene Merkelzellkarzinom mit Chemotherapie behandelt. Dieser Ansatz würde Tumore in über der Hälfte der Fälle verkleinern, aber der Nutzen würde im Durchschnitt nur drei Monate anhalten. Als der Krebs zurückkehrte, war er gegen viele Medikamente resistent, und das Immunsystem war durch die Chemotherapie unterdrückt worden, was die Probleme für einen sehr immunempfindlichen Krebs verschlimmerte. Checkpoint-Inhibitoren sind jedoch eine aufregende neue Klasse von Immuntherapien (Behandlungen, die die Fähigkeit des Immunsystems stärken, eine Krankheit zu bekämpfen) und sind zum Behandlungsstandard für fortgeschrittenes MCC geworden. Indem sie Proteinrezeptoren blockieren, die normalerweise das Immunsystem in Schach halten, regen diese Medikamente die T-Zellen an, den Tumor zu bekämpfen.
Im März 2017 hat die US Food and Drug Administration (FDA) ein immunstimulierendes Medikament, Avelumab (Bavencio), für die Behandlung von Erwachsenen und pädiatrischen Patienten ab 12 Jahren mit metastasiertem MCC zugelassen. Die FDA-Zulassung, die allererste für fortgeschrittenes MCC, basierte auf Daten aus einer klinischen Studie, in der 33 Prozent der Patienten eine vollständige oder teilweise Schrumpfung ihrer Tumore erlebten, obwohl sie alle zuvor eine Chemotherapie für ihr MCC erhalten hatten. Nachfolgende Studien mit Avelumab haben höhere Ansprechraten gezeigt, wenn es als Erstlinientherapie (vor einer Chemotherapie) verabreicht wurde, wobei etwa 50 % der Patienten davon profitierten.
Avelumab wird intravenös injiziert und stimuliert T-Zellen, indem es ein Molekül namens PD-L1 (programmierter Todesligand 1) blockiert, das sich mit PD-1 verbindet, um diese kritischen Immunzellen zu hemmen.
In 2018, das von der FDA zugelassene Pembrolizumab (Keytruda) zur Behandlung von MCC, nach einer Studie mit Patienten mit rezidivierendem lokal fortgeschrittenem oder metastasiertem MCC, die keine Behandlung erhalten hatten früher systemische Therapie für die Krankheit zeigte eine 56 Prozent Ziel Rücklaufquote (ORR).
In 2023, die FDA beschleunigte Zulassung erteilt Retifanlimab-dlwr, auch eine PD-1 Hemmer, als Behandlung für Erwachsene mit metastasierender oder rezidivierender lokaler Fortschrittd MCC. Es ist soSicherheit und Wirksamkeit basierten auf Daten aus der POD1UM-201-Studie, in der die Behandlung von Erwachsenen mit metastasiertem oder rezidivierendem lokal fortgeschrittenem MCC untersucht wurde, die zuvor keine systemische Therapie gegen die Krankheit erhalten hatten. Diese Patienten zeigten eine ORR von 52 Prozent.
Früher fühlte ich mich hoffnungslos für Patienten mit metastasiertem MCC. Nun, es ist eindeutig nicht hoffnungslos.
F: Gibt es eine bevorzugte Reihenfolge, in der die Behandlungen jetzt durchgeführt werden sollten? Müssen Sie zuerst eine Chemotherapie oder Bestrahlung verabreichen, bevor Sie eine der Checkpoint-Blockade-Therapien anwenden?
A: Bis vor kurzem war die Chemotherapie die Therapie an vorderster Front. Aber wenn Sie fortgeschrittenes MCC vor der Chemotherapie mit einem Checkpoint-Inhibitor behandeln, sprechen etwa 60 Prozent der Patienten an. Wenn Sie warten, bis der Patient eine Runde Chemotherapie versagt hat, scheinen etwa 40 Prozent der Patienten anzusprechen. Und nach zwei oder mehr Runden Chemotherapie sprechen etwa 20 Prozent der Patienten an. Daher scheint es jetzt normalerweise der richtige Ansatz zu sein, zuerst das immunstimulierende Medikament zu verwenden und dann basierend auf der Reaktion zu entscheiden, was als nächstes zu tun ist. Einige Patienten zeigen ein vollständiges Ansprechen mit vollständiger Remission der Krankheit. Die Tumore einiger Patienten sprechen teilweise an, wobei das Tumorvolumen oft um 70 Prozent abnimmt, was immer noch eine starke Reaktion darstellt. Viele dieser Patienten haben am Ende ein geringes Krankheitsniveau, das ihre Gesundheit überhaupt nicht beeinträchtigt. Eine Frau, die ich kürzlich behandelte, hatte ein Jahr lang eine partielle Remission, dann änderte sie sich zu einer vollständigen Remission. Aber normalerweise, wenn das Medikament wirken soll, kommt die Reaktion schnell (innerhalb von 1-2 Monaten), und die meisten Reaktionen halten weit über ein Jahr an. Wir sind jedoch unsicher, was passieren wird, wenn das Medikament abgesetzt wird.
Da Avelumab jetzt von der FDA für MCC zugelassen ist, das zuvor mit oder ohne Chemotherapie behandelt wurde, wird es jetzt bevorzugt als Erstlinientherapie für metastasiertes MCC verwendet, während eine Chemotherapie in den meisten Fällen nicht bevorzugt wird. Aktuelle Daten deuten darauf hin, dass eine Immuntherapie besser wirkt, wenn sie vor einer Chemotherapie gegeben wird, die das Immunsystem tendenziell unterdrückt und Tumore widerstandsfähiger gegen eine Vielzahl von Behandlungen macht.
Obwohl die Chemotherapie nicht mehr die übliche Behandlung an vorderster Front ist, kann die Bestrahlung in einigen Fällen früh im Spiel vorteilhaft eingesetzt werden. Es kann gut mit der Immuntherapie zusammenwirken. Das Immunsystem eliminiert kleine Tumore besser als große Tumore, und Bestrahlung kann Tumore effektiv schrumpfen lassen. Wenn das Ansprechen auf die Immuntherapie nicht vollständig ist, können einzelne nicht ansprechende Läsionen manchmal mit ein wenig Strahlentherapie behandelt werden, um die Arbeit des Immunsystems zu erleichtern.
F: Was ist mit den anderen von der FDA zugelassenen Checkpoint-Blockade-Therapien für Melanome, Nivolumab (Opdivo®) und der Kombination Ipilimumab (Yervoy®)-Nivolumab? Werden sie auch wegen MCC versucht?
A: Es gibt immer mehr Daten darüber, wie die „ipi-nivo“-Kombination bei MCC funktioniert. Seine Hauptanwendung war bei Patienten, die nicht auf ein einzelnes immunstimulierendes Mittel (Avelumab oder Pembrolizumab) ansprechen. Bei solchen „refraktären“ Patienten scheint die Ipi-nivo-Kombination in etwa 20 bis –30 Prozent der Fälle helfen zu können. Im Gegensatz dazu wird ipi-nivo in der Regel anfänglich nicht verwendet, da die Ansprechrate von etwa 60 Prozent für Pembrolizumab oder Avelumab allein ziemlich hoch ist und die Einbeziehung von Ipilimumab (Yervoy) in die Immuntherapie bekanntermaßen erhebliche Nebenwirkungen im Vergleich zu einer einzelnen PD hinzufügt -1-Pathway-Medikament (wie Avelumab oder Pembrolizumab.).
F: Was passiert als nächstes, wenn keine der anfänglichen Checkpoint-Therapien funktioniert?
A: Dies ist ein riesiges Interessens- und Forschungsgebiet. Wie oben erwähnt, kann die „ipi-nivo“-Kombination bei etwa 20 bis -30 Prozent der MCC-Fälle helfen, die nicht auf eine einzelne Immun-Checkpoint-Therapie ansprechen. Es ist auch möglich, lokale Injektionen von immunstimulierenden Therapien mit einem systemischen Mittel wie einer Immuntherapie zu kombinieren. Andere Ansätze, die untersucht werden, umfassen die Verabreichung genetisch optimierter krebsspezifischer Killer-T-Zellen an Patienten, ähnlich den „CAR-T“-Zellen, die sich bei bestimmten Blutkrebsarten als vorteilhaft erwiesen haben.
F: Sie sagten, Sie erwarten, dass etwa die Hälfte der Patienten mit den Checkpoint-Blockade-Therapien gut abschneiden. Das deutet darauf hin, dass etwa die Hälfte dies nicht tun wird. Da es sich um teure Behandlungen mit einigen potenziell schwerwiegenden Nebenwirkungen handelt, gibt es eine Möglichkeit, im Voraus zu wissen, welche Patienten davon profitieren, damit Sie die vorhergesagten Non-Responder mit einer vorteilhafteren Behandlung beginnen können?
A: Obwohl mehr als die Hälfte der Patienten ansprechen, schreitet der Krebs bei etwa 40 Prozent der Patienten weiter fort, als ob Sie überhaupt keine Behandlung durchführen würden. Wir und viele andere arbeiten sehr hart daran, dieses Problem zu lösen, und ich freue mich, sagen zu können, dass es in diesem Bereich nach mehr als fünf Jahren Arbeit Fortschritte gibt. Es scheint, dass Patienten, die viele krebsspezifische T-Zellen in ihrem Blut haben, mit weitaus größerer Wahrscheinlichkeit auf Checkpoint-Inhibitoren ansprechen als diejenigen, die dies nicht tun. Faszinierenderweise sagt die Anzahl krebsspezifischer T-Zellen in den Tumoren keine Reaktion voraus. Um eine militärische Schlachtanalogie zu verwenden, scheint es, dass die Anzahl effektiver Truppen, die als Ersatz (im Blut) verfügbar sind, entscheidend für den Sieg des Krieges ist. Im Gegensatz dazu ist die Zahl, die wir auf dem Schlachtfeld (im Tumor) finden, nicht wichtig. Diese Ergebnisse deuten darauf hin, dass wir, wenn wir die Anzahl der krebsspezifischen T-Zellen erhöhen können, die dem Patienten zur Verfügung stehen, ihm möglicherweise helfen können, den Krebs besser zu bekämpfen.
F: Wie sieht es nach einer Behandlung aus? Gibt es eine Möglichkeit, frühzeitig zu wissen, ob der Krebs zurückkommt?
A: Wir haben in diesem Bereich aufregende Fortschritte gemacht. Unser Team hat einen Bluttest entwickelt, der nach bestimmten Merkelzell-Polyomavirus-Antikörpern im Blut sucht, damit wir eventuelle Rezidive frühzeitig erkennen können, wenn der Tumor besser behandelbar ist (vgl www.merkelcell.org/sero).
Im Jahr 2008 fanden Patrick S. Moore, MD und Yuan Chang, MD heraus, dass die meisten Merkelzellkarzinome teilweise durch ein Virus verursacht werden. (Auch Sonnenlicht spielt oft eine Rolle.) Wir finden dieses Merkelzell-Polyomavirus in etwa 80 Prozent der MCC-Tumoren. Wenn dieses Virus Zellen infiziert, produziert es Onkoproteine (krebsfördernde Proteine), die dazu führen können, dass die Zellen unkontrolliert wachsen. Wir führen den Bluttest in unterschiedlichen Intervallen durch, beginnend mit dem Zeitpunkt der Diagnose, und wenn die Anzahl der Antikörper gegen diese Polyomavirus-Proteine jemals ansteigt, deutet dies stark darauf hin, dass der Patient einen Rückfall hat.
Wir verwenden diesen Test jetzt routinemäßig, da er bei der Behandlung von Patienten im Laufe der Zeit sehr hilfreich ist. Ungefähr die Hälfte der Patienten produziert keinen dieser Antikörper, und sie haben tatsächlich ein um etwa 40 Prozent höheres Risiko, dass ihr MCC erneut auftritt, als diejenigen, die die Antikörper produzieren, daher wissen wir, dass wir ihnen mit anderen Ansätzen genau folgen müssen. Für Patienten, die die Antikörper bilden, ist es relativ einfach: Kommt der Krebs nicht zurück, fallen die Antikörper schnell ab und sind in den meisten Fällen ein Jahr nach der Behandlung nicht mehr nachweisbar. Wenn MCC zurückkommt, steigen die Antikörper. Es gibt uns eine große Chance, Rezidive früh zu entdecken, wenn sie extrem behandelbar sind: Die Behandlung einer Traube anstelle einer Grapefruit (in Bezug auf die Krebsgröße) macht einen großen Unterschied. Und bei einem Patienten, dessen Antikörper weiter sinken, gibt uns der Bluttest große Gewissheit, dass der Krebs nicht wiederkehrt, sodass wir den Einsatz kostspieliger bildgebender Scans überspringen oder reduzieren können.
Ab 2022 sind wir an der Entwicklung eines weiteren Tests beteiligt, der DNA-Stücke des Krebses erkennt, die im Blut herumschwimmen. Dies wird als „zirkulierender Tumor-DNA“-Test bezeichnet. Es wurde für Krebsarten, einschließlich Brust- und Dickdarmkrebs, eingesetzt. Es scheint besonders gut für MCC zu funktionieren. Ein großer Vorteil dieses Tests ist, dass er auch bei Patienten funktioniert, die keine Antikörper gegen das Merkel-Virus bilden. Daher sollten praktisch alle MCC-Patienten einen Bluttest haben, der in der Regel genauer und empfindlicher ist als Körperscans
F: Wie entscheiden Sie, nachdem Sie MCC-Patienten behandelt haben, wie oft Sie sie sehen und wie hoch das Risiko ist, dass der Krebs erneut auftritt?
A: Im April 2022 wir haben kürzlich berichtet dass das Gesamtrisiko eines MCC-Rückfalls 40 Prozent beträgt; Dies ist eine deutlich höhere Rate als bei den häufigeren Hautkrebsarten. Darüber hinaus ist klar, dass das Krebsstadium eines Patienten bei der Vorstellung und andere Risikofaktoren das eigene Risiko eines MCC-Rezidivs stark beeinflussen. Zu diesen Faktoren gehören Immunsuppression, männliches Geschlecht und fortgeschrittenes Alter, die alle das Wiederholungsrisiko erhöhen. Angesichts der Tatsache, dass 95 Prozent der Rezidive in den ersten drei Jahren nach der Diagnose auftreten, ist die Zeit seit der Diagnose ein sehr wichtiger Faktor, der die verbleibende Chance eines Patienten bestimmt, dass sein MCC noch auftritt. Dies wiederum ist sehr hilfreich bei der Bestimmung, wie aggressiv Patienten überwacht werden sollten.
Wir haben einen webbasierten „Risikorechner“ erstellt. die diese verschiedenen Faktoren berücksichtigt. Es ist erhältlich über www.merkelcell.org/recur.
In unserer täglichen Praxis hat sich dies als unglaublich nützlich erwiesen. Wenn Patienten Sie beispielsweise zu ihrer einjährigen Nachsorgeuntersuchung aufsuchen, ist es jetzt möglich, ihnen mitzuteilen, wie hoch ihr „Rest“-Erkrankungsrisiko im Vergleich zu ihrer Wahrscheinlichkeit zu Beginn der Überwachung ist.
Generell glauben wir heute, dass wir Patienten nicht mehr so viele Jahre lang so engmaschig überwachen müssen wie früher. MCC scheint nicht wie ein Melanom zu sein, das oft fünf oder zehn Jahre nach der Diagnose wieder auftritt. Wenn es bei MCC erneut auftritt, dauert es normalerweise zwei bis drei Jahre. Daher denken wir jetzt, dass eine intensive Nachsorge über zwei oder drei Jahre normalerweise angemessen ist, mit einem deutlich weniger aggressiven Zeitplan bis etwa zum fünften Jahr.
F: Machen andere neue Behandlungsformen einen Unterschied?
A: Die Checkpoint-Blockade-Immuntherapien waren bahnbrechend, und keine anderen getesteten Therapien haben bisher einen solchen Unterschied gemacht. In Kombination mit der Checkpoint-Therapie setzen wir nun aber patienteneigene T-Zellen ein, um den Krebs zu bekämpfen. In einigen Fällen „programmieren“ wir die Zellen des Patienten so, dass sie den Krebs angreifen, indem wir das Virus erkennen. In anderen Fällen finden und vermehren wir eigene Merkelvirus-spezifische T-Zellen. Dies kann das Immunsystem stärken, und die Kombination dieser Therapie mit einer Checkpoint-Blockade-Therapie kann wirksamer sein als jeder Ansatz allein.
Wir prüfen auch die Kombination einiger intraläsionaler Therapien mit den Checkpoint-Blockade-Therapien. In kleinen MCC-Studien haben sie oft die injizierten Tumore geschrumpft oder beseitigt und einige andere Tumore im ganzen Körper reduziert. Studien laufen, aber es scheint wahrscheinlich, dass einige dieser „lokalen“ Immunstimulatoren, die zusammen mit Immun-Checkpoint-Mitteln verabreicht werden, dazu beitragen werden, höhere Ansprechraten zu erzielen als die selbst verabreichten Checkpoint-Mittel.
Veröffentlicht am 7. November 2016. Aktualisiert am 21. September 2022.
