El Carcinoma de Células de Merkel
¿Qué es el carcinoma de células de Merkel?
El carcinoma de células de Merkel (CCM) es un cáncer de piel agresivo y poco frecuente con alto riesgo de recidiva y propagación (metástasis). La mayoría de los casos de recidiva tienen lugar dos años después de que el primer tumor haya sido diagnosticado. Mientras que esta enfermedad es 30 veces menos frecuente que el melanoma (se estima que hay 0,24 casos por cada 100.000 personas en E.E.U.U.), su tasa de mortalidad es de 1 de cada 3 casos, comparado con 1 de cada 6 para el melanoma.
El CCM ocurre con más frecuencia en áreas de la piel expuestas al sol en individuos de piel blanca mayores de 50 años. Su nombre se debe a la similitud de estas células cancerosas con las células de Merkel en la piel, que se considera que están relacionadas con el sentido del tacto. Las células normales de Merkel fueron descritas hace más de 100 años por Friedrich Sigmund Merkel.
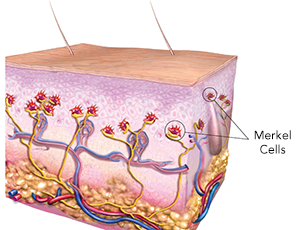
Figura 1: Células de Merkel normales en la piel: En esta ilustración (sección vertical de la piel) se ven células de Merkel normales (en rojo), conectadas con los nervios (en amarillo). En la figura se observan la epidermis (en el tercio superior), la dermis (tercio medio) y la capa de tejido adiposo profundo, o hipodermis, que contiene el tejido graso y el plexo arteriovenoso. Las arterias destacan en rojo y las venas en azul. Figure Copyright by Paul Nghiem & Quade Medical Group.
¿Qué origina el carcinoma de células de Merkel? – Causas
La inmunodepresión y el CCM están estrechamente relacionados. Las personas con un sistema inmunológico crónicamente deprimido (como pacientes con VIH, o aquellos que han recibido un trasplante de órgano y deben tomar medicamentos inmunosupresores) son 15 veces más susceptibles de desarrollar CCM que las personas que no están inmunodeprimidas. El carcinoma de células de Merkel ocurre a una edad significativamente más temprana en pacientes con trasplante de órganos e infecciones por VIH; alrededor de un 50% de los casos de CCM en pacientes inmunodeprimidos ocurre antes de los 50 años de edad.
Diversos estudios también apuntan a una estrecha relación entre el CCM y la exposición a la luz ultravioleta (UV). El CCM está muy vinculado al carcinoma espinocelular o de células escamosas (CCS), el carcinoma basocelular o de células basales (CCB) y a la enfermedad de Bowen (que es una forma precoz y superficial de CCS, para algunos una carcinoma “in situ”), los cuales son causados, en la mayoría de los casos, por la exposición a la luz UV. Los pacientes con psoriasis que reciben tratamiento con rayos UVA y psoralenos (sensibilizantes que potencian el efecto de la luz UV) tienen una incidencia de CCM 100 veces mayor a la de la población general.
De hecho, la exposición a la luz UV es un peligro doble: no sólo daña la piel, aumentando el riesgo de cáncer de piel, sino que también deprime el sistema inmunológico, reduciendo su capacidad para reparar la piel dañada y para reconocer y rechazar células cancerosas y otras enfermedades.
Además de la radiación UV, algunos medicamentos administrados a los pacientes con trasplantes de órganos e infectados por el virus de inmunodeficiencia humana (VIH), también hay enfermedades autoinmunes, como la artritis reumatoide, y otras enfermedades graves, como la leucemia linfocítica crónica o los linfomas, que pueden deprimir gravemente el sistema inmunológico. Los pacientes con estos tipos de inmunodepresión tienen el doble de probabilidades de fallecer a causa del CCM en comparación con individuos que gozan de un sistema inmunológico normal. Esto sugiere que el sistema inmunológico no sólo previene el desarrollo de CCM, sino que también ayuda a impedir la propagación de sus células cancerosas.
En 2008, un grupo de científicos de la Universidad de Pittsburgh descubrió un “poliomavirus de células de Merkel”, un virus humano presente en aproximadamente el 80% de los CCM, pero en menos del 10% de los melanomas y otros cánceres de piel. A los 20 años de edad, la mayoría de las personas ya han estado expuestas en algún momento a poliomavirus (miembros de la familia de los virus de ADN de doble cadena). Cuando el poliomavirus de células de Merkel infecta una célula, éste produce proteínas que pueden causar un crecimiento celular (división) descontrolado, provocando el cáncer. Sin embargo, alrededor del 20% de los tumores de CCM no tienen este virus, lo cual indica que su presencia no es necesaria en todos los casos de CCM. Además, la mayoría de las personas tienen el poliomavirus toda su vida y nunca desarrollan CCM. Es posible que cuando alguien tiene el poliomavirus sean necesarios otros factores, como la exposición a la luz UV y la inmunodepresión, para iniciar el crecimiento del cáncer.
Carcinoma de células de Merkel – Factores de riesgo y señales de advertencia
Los principales factores de riesgo para el carcinoma de células de Merkel incluyen:
- ser mayor de 50 años de edad (la mayoría de los pacientes tienen más de 70 años)
- ser varón
- tener piel clara
- exposición a la luz ultravioleta solar o de camas de bronceado
- inmunodepresión.
Los carcinomas de células de Merkel son normalmente curables si se detectan y tratan en las primeras fases de su desarrollo. Sin embargo, al ser frecuentemente agresivos y de rápido crecimiento, es de vital importancia detectarlos y extirparlos lo antes posible.
Estos tumores se presentan normalmente como elementos nodulares firmes e indoloros localizados en un área expuesta al sol (un 48% de los casos aparecen en la cabeza y el cuello, y con frecuencia en los párpados). Generalmente son rojos, azules o del color de la piel, y pueden ser de diferente tamaño, aunque lo más frecuente es que no superen los 20 mm de diámetro. El tamaño promedio cuando se detecta por primera vez es de aproximadamente el diámetro de una moneda de diez centavos estadounidense (17 mm).
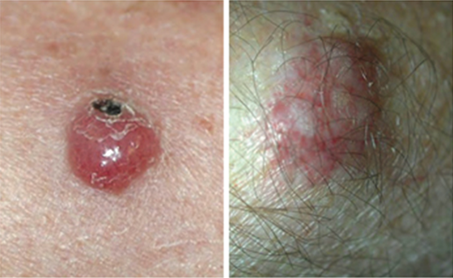
Figura 2. (izquierda) Recidiva local de carcinoma de células de Merkel en la frente.
Figura 3. (derecho) Carcinoma de células de Merkel, como tumor primario (“de novo”), en tercio inferior de brazo.
Es fundamental que usted y su médico estén alerta sobre estos signos y también sobre la presencia de posibles lesiones nuevas o cambiantes en su piel, tanto si se presentan y evolucionan de forma rápida como si no, especialmente si ya ha padecido un CCM. Preste especial atención a cualquier área tratada en el pasado, y si detecta algo sospechoso, muéstreselo a su médico inmediatamente.
Algunos médicos utilizan el acrónimo “AEIOU” para resumir la combinación de factores de riesgo y los signos de advertencia que indican la necesidad de que se les realice un examen minucioso con el objetivo de conseguir un diagnóstico precoz:
- A: Asintomático/falta de sensibilidad
- E: Expansión rápida
- I: Inmunodepresión
- O: Mayores de 50 años (older)
- U: Ultravioleta-exposición/piel blanca
Carcinoma de células de Merkel – Fases
Los médicos suelen recomendar una técnica llamada biopsia de ganglio linfático centinela (BGLC) en pacientes con carcinoma de células de Merkel, independientemente del tamaño del tumor, para determinar si la enfermedad se ha propagado (metástasis) a los ganglios linfáticos. Como esta técnica es mínimamente invasiva, con bajo riesgo de efectos secundarios, se considera muy importante para determinar el pronóstico de un paciente, ya que una vez alcanzado el ganglio linfático, las células cancerosas pueden propagarse fácilmente a través de los vasos linfáticos, pasar al torrente sanguíneo y circular por todo el cuerpo. Estos ganglios son pequeñas protuberancias en el sistema linfático, que es donde se forman los linfocitos (las células blancas de la sangre) y se filtra la linfa, un fluido incoloro que contiene las células blancas. La linfa baña los tejidos, drenando al torrente sanguíneo a través de los vasos linfáticos.
¿Qué ocurre durante una Biopsia del Ganglio Centinela?
- Para realizar una biopsia del ganglio centinela, el equipo médico comienza con la identificación (localización) de los ganglios centinela, utilizando una técnica llamada linfoescintigrafía, o mapeo linfático. Se inyecta un marcador radiactivo y/o un colorante azul en el área del tumor, que circula por los vasos linfáticos drenando, a través de ellos, desde el sitio de la inyección a los ganglios linfáticos locales. Posteriormente, con un instrumento que detecta el marcador, se efectúa un mapeo de la ruta desde el tumor hasta los ganglios linfáticos centinela, que son los primeros (hasta tres) ganglios de la vía linfática. Lo más predecible es que cualquier célula cancerosa que se propague desde el tumor siga la misma ruta.
- El cirujano extirpa los ganglios centinela. Después, en un Laboratorio de histopatología, un médico los examina al microscopio, buscando células cancerosas.
- Si la biopsia revela cualquier célula cancerosa, el cirujano extirpa todos los demás ganglios locales de la vía linfática, o, en ciertos casos, utiliza terapia de radiación para destruirlos.
Beneficios de la biopsia de ganglios linfáticos centinela
Sigue siendo controvertido el hecho de si la biopsia de ganglios linfáticos centinela, seguida de la extirpación de todos los ganglios locales de la vía linfática, si la biopsia revela células cancerosas, realmente alarga la supervivencia. Sin embargo, los médicos aún recomiendan esta técnica de forma rutinaria, ya que las células cancerosas se detectan en los ganglios linfáticos regionales en uno de cada tres pacientes con CCM, y a menudo el reconocimiento médico no es suficiente para detectar la enfermedad. Los médicos consideran que el mapeo linfático y la BGLC son de gran importancia para los pacientes de CCM:
- El mapeo linfático identifica la región donde es más probable que las células cancerosas se hayan podido propagar.
- Un ganglio centinela revela “micrometástasis”, células metastásicas que no son visibles al ojo humano y que no se pueden detectar en un reconocimiento médico de rutina.
- Los resultados de la BGLC ayudan al médico a determinar el pronóstico: si los ganglios centinela son negativos, los pacientes tienen un 80% de probabilidad de sobrevivir cinco años. Si son positivos, los pacientes tienen un 50% de probabilidad de sobrevivir cinco años.
- Los resultados también ayudan a los médicos a evaluar la fase de avance (estadio) que el cáncer ha alcanzado, y si es necesario un tratamiento adicional. Y también son de utilidad en la elección del tratamiento adecuado.
- Extirpar los ganglios cancerosos, y/o establecer un curso de terapia de radiación, ayuda a prevenir la recidiva local.
Fases del carcinoma de células de Merkel
Una vez completada la biopsia del tumor original y de los ganglios centinela, y cualquier otro análisis realizado (incluyendo pruebas de imagen y análisis de sangre), el oncólogo determinará la fase de la enfermedad. La fase representa el avance y la propagación del cáncer, y considera factores como:
- El grosor del tumor, la ulceración y la tasa de crecimiento (tasa mitótica).
- Si el cáncer ha alcanzado o no los ganglios adyacentes y cuántos ganglios están implicados.
- Si las células cancerosas se han propagado o no a zonas distantes más allá de los ganglios linfáticos.
- Qué zonas del cuerpo y qué órganos están implicados.
La elección del tratamiento depende directamente de la fase que el cáncer ha alcanzado. No existe un sistema de fases universal para el CCM, pero hoy día, el sistema más usado es el sistema TNM de la American Joint Committee on Cancer (AJCC), donde la T representa el tumor primario (original) (su tamaño, su tasa de crecimiento y otros factores), la N indica la propagación a los nódulos (ganglios) linfáticos locales (y el alcance de la implicación ganglionar) y la M corresponde a metástasis distantes (propagadas por áreas del cuerpo, ganglios linfáticos y órganos más allá de los ganglios linfáticos locales). El sistema de la AJCC incluye cinco fases:
- Fase 0: Tumores “in situ” (tumores superficiales que no han penetrado más allá de la epidermis, la capa más externa de la piel).
- Fase I y Fase II: Tumores que no se sabe si han avanzado hasta los ganglios linfáticos locales, donde la Fase I incluye tumores relativamente pequeños y de bajo riesgo, y la Fase II incluye tumores más grandes y/o de mayor riesgo.
- Fase III: Tumores que se sabe que han alcanzado los ganglios linfáticos locales, pero no más allá.
- Fase IV: Metástasis a distancia. Tumores cuyas células cancerosas ya se han propagado a otras áreas del cuerpo distantes, a ganglios linfáticos no regionales/locales y a otros órganos vitales (los pulmones son las órganos más frecuentemente afectados).
Además, cada una de estas fases es subdividida de forma más precisa, de menor a mayor riesgo, dependiendo de diferentes características del tumor primario, metástasis ganglionar (nódulo linfático) y/o metástasis distantes (p.e. M1b. metástasis pulmonar).
Carcinoma de células de Merkel – Opciones terapéuticas
El tratamiento del carcinoma de células de Merkel depende de la fase en la que se encuentre la enfermedad, además de la salud general del paciente. Hoy en día, los tratamientos básicos para el CCM son: extirpación quirúrgica, radiación y quimioterapia.
En todas las fases del CCM, los médicos recomiendan la extirpación completa del tumor primario (original), confirmándose su diagnóstico por el inmediato examen histopatológico. Después de la extirpación, si el riesgo de recidiva o propagación a los ganglios linfáticos locales es alto (debido a diversos factores como un tumor primario de gran tamaño, extirpación incompleta o que el paciente se encuentra en estado de inmunodepresión), el médico recomendará, en la mayoría de los casos, que la tumoración sea tratada con un curso de radiación. De hecho, muchos médicos recomiendan un curso de radiación para todos los pacientes de CCM. Esto puede destruir cualquier célula cancerosa no detectable por reconocimiento médico y puede ayudar a prevenir la recidiva o la propagación del cáncer a los ganglios linfáticos locales o más allá. El carcinoma de células de Merkel es especialmente sensible a la radiación.
Si el cáncer ha alcanzado la vía de ganglios linfáticos locales, los médicos, generalmente, también extirpan y/o irradian todos los ganglios del sistema linfático afectado, reduciendo así el riesgo de recidiva, lo que a su vez puede prevenir metástasis a distancia. En la mayoría de los casos, los pacientes que no muestran una clara invasión de los ganglios linfáticos deberían someterse a un procedimiento llamado biopsia de los ganglios linfáticos centinela (BGLC) para verificar si las células cancerosas han alcanzado o no la vía de los ganglios linfáticos locales. A diferencia de otros cánceres de piel, con frecuencia los CCM ya se han propagado a los ganglios linfáticos adyacentes, o más allá, antes de llegar al diagnóstico, ya que, a veces, se comprueba engrosamiento de los ganglios en el reconocimiento médico. Incluso un CCM pequeño tiene un 30% de probabilidad de haberse propagado a los ganglios linfáticos adyacentes antes de hacerse el diagnóstico. (Si comparamos este grado de propagación con el de otros tumores cutáneos como los melanomas, comprobaremos que la probabilidad de que un melanoma se propague a los ganglios linfáticos adyacentes antes del diagnóstico es sólo un 1%).
Los resultados de la biopsia de los ganglios centinela son importantes para ayudar al médico a determinar el pronóstico del paciente y a elegir el tratamiento correspondiente. Si la histopatología es negativa, no se necesitará tratamiento adicional. Si es positiva, los médicos suelen extirpar el resto de los ganglios de la vía linfática y con frecuencia también realizan un curso de radiación sobre la propia vía después de eliminar todos los ganglios linfáticos. Dependiendo de los resultados de pruebas adicionales, pueden también considerarse otros tratamientos.
Los médicos suelen recomendar quimioterapia sólo para pacientes en los que el cáncer se haya propagado a zonas distantes o a órganos como pulmones o hígado. Varios tipos de quimioterapia se han utilizado para casos avanzados de CCM, con éxito variado (y a menudo limitado). Por desgracia, suelen tener efectos secundarios. No hay estudios clínicos controlados que muestren la prolongación de la supervivencia con ninguno de estos tipos de quimioterapia, pero pueden determinar con frecuencia remisiones cortas. Los médicos también pueden utilizarlas para eliminar o reducir lesiones específicas con el fin de disminuir el dolor y aumentar la movilidad del paciente.
Inmunoterapia
Fármacos inhibidores del punto de control inmunitario
Investigaciones recientes han logrado el primer éxito significativo en el tratamiento del carcinoma de células de Merkel (CCM) en estadio IV, con una forma de inmunoterapia llamada “terapia de bloqueo del punto de control”. En marzo de 2017, la Administración para Medicamentos y Alimentos de los Estados Unidos (FDA) aprobó el tratamiento con avelumab (nombre comercial Bavencio) para terapéutica mediante la inhibición del punto de control inmunitario tanto en adultos como en niños de más de 12 años con CCM. La aprobación de la FDA de este primer medicamento para el tratamiento del CCM avanzado, se basó en datos de un ensayo clínico en el que se comprobó una reducción total o parcial de los tumores en el 33% de los pacientes.
Las inmunoterapias con “fármacos inhibidores del punto de control inmunitario” inhiben ciertas moléculas que bloquean o “controlan” la producción de células T previniendo reacciones inflamatorias y autoinmunes excesivas que, en condiciones normales, pueden ser potencialmente peligrosas. Al bloquear estas moléculas inhibidoras, los fármacos liberan en oleadas células T para atacar a las células del CCM.
Avelumab bloquea en las células tumorales el ligando del PD-1 (muerte programada-1)(PD-L1), evitando que se una a este PD-1, con lo que se liberan las células T para combatir el CCM. En el ensayo de avelumab, las respuestas duraron más de 6 meses en el 86% y más de 12 meses en el 45% de los pacientes que respondieron.
Otra terapia de bloqueo de puntos de control, pembrolizumab (nombre comercial Keytruda), también ha producido resultados experimentales prometedores en pacientes con CCM por lo que podría ser eventualmente aprobada por la FDA. Pembrolizumab fue aprobado previamente para el tratamiento de pacientes con melanoma avanzado, prolongado la vida de estos pacientes durante muchos años, lo que lleva a considerarla como causante de remisiones a largo plazo.
El pembrolizumab bloquea la molécula inhibidora de la inmunidad PD-1, liberando así intermitentemente o en oleadas células T para atacar a las células cancerosas. En un pequeño estudio inicial de 26 pacientes con CCM avanzado, 14 (56%) respondieron al tratamiento con pembrolizumab, y en cuatro pacientes se logró remisión completa. La mayoría de los pacientes que respondieron tenían el poliomavirus de células de Merkel, lo que sugiere que los antígenos del virus pueden mejorar la respuesta terapéutica. Aunque el estudio no fue diseñado específicamente para determinar si el pembrolizumab podría bloquear el poliomavirus-MCC, los resultados demostraron que el tratamiento tenía este efecto, por lo que habrá que investigar en estudios futuros si este y otros tratamientos pueden tener como objetivo al poliomavirus.
El 30 de mayo de 2017, un equipo de investigadores de la Universidad Fred Hutchison y de la Universidad de Washington en Seattle informó de los magníficos resultados obtenidos en un pequeño estudio que combinaba avelumab con otros dos tratamientos (terapia de transferencia de células T autólogas y radiación u otra inmunoterapia como el interferón). ). En tres de cada cuatro pacientes con CCM metastásico en estadio IV tratados con esta combinación experimental se demostró remisión completa después del tratamiento, sin que hubiera signos de cáncer. En la terapia de transferencia de células T autólogas, los investigadores extraen de la sangre de los pacientes un cúmulo de células T que reconocen el CCM, las multiplican en el laboratorio y luego las reinyectan en estos pacientes para aumentar su agresividad hacia las células de CCM. Cuando agrega el avelumab, parece que las células T mejoran en rapidez y agresividad.
Un estudio previo de cuatro pacientes en los que se combinó la terapia de transferencia de células T con radiación o interferón, pero sin incluir avelumab, no obtuvo tan buenos resultados, puesto que la enfermedad progresó en tres de los pacientes, dos de los cuales ya han fallecido.
Seguimiento
Si ha recibido tratamiento para un CCM, usted y su médico deberían controlar su piel el resto de su vida. El seguimiento que se recomienda después del tratamiento es una vez al mes durante los primeros seis meses, cada tres meses durante los próximos dos años y a partir de ahí cada seis meses.
Dificultades en el diagnóstico y el tratamiento
Diagnosticar y abordar el carcinoma de células de Merkel es difícil. Tanto los pacientes como los médicos pueden confundir al principio estos tumores con lesiones benignas. En efecto, el estudio histopatológico de la tumoración extirpada demostró que el 58% habían sido diagnosticados previamente como tumores benignos, siendo el diagnóstico más frecuente el de quiste o foliculitis (hinchazón causada por inflamación de folículos pilosos).
En algunos casos, el tumor de células de Merkel aparece en zonas que escapan a la detección, lo que retrasa aún más el diagnóstico: un 5% de los casos de CCM ocurre en mucosas, como la boca, la cavidad nasal y la laringe, donde es difícil de detectar antes de que la enfermedad haya avanzado. En un estudio, el 14% de los casos de CCM fueron descubiertos inicialmente en los ganglios linfáticos, sin haber identificado nunca la localización del tumor primario.
Ya que el CCM es un cáncer especialmente agresivo, el retraso en la detección pueden llevar a un diagnóstico y tratamiento tardíos, en cuyo caso las recidivas son frecuentes y es más difícil conseguir que el tratamiento tenga éxito.
Guías de prevención
Un funcionamiento inmunológico reducido contribuye en gran medida al desarrollo del carcinoma de células de Merkel, por lo que, como en todos los casos, es importante adoptar un estilo de vida saludable y mantener el sistema inmunológico fuerte. Además, ya que la exposición a la radiación ultravioleta (UV) se considera la causa primaria de esta enfermedad, es importante prevenir la sobreexposición a UV, especialmente si ya se ha tenido un CCM, o si algún familiar cercano ha tenido la enfermedad o cualquier otro cáncer de piel.
Para protegerse, haga estos hábitos parte de su rutina diaria de salud:
- Busque la sombra, sobre todo entre las 10:00 y las 16:00 horas.
- Evite quemarse.
- Evite el bronceado y nunca utilice camas de bronceado UV.
- Cúbrase con ropa, incluyendo un sombrero de ala ancha y gafas de sol que bloqueen la luz UV.
- Utilice un protector solar de espectro amplio (UVA/UVB) con un Factor de Protección Solar(FPS) del 15 o superior todos los días. Para actividades en exterior prolongadas, utilice un protector solar resistente al agua de espectro amplio (UVA/UVB) con un FPS de 30 o superior.
- Aplique dos cucharadas pequeñas de protector solar 30 minutos antes de salir a la calle. Vuelva a aplicar la misma cantidad cada dos horas o inmediatamente después de nadar o haber sudado excesivamente.
- Mantenga a los recién nacidos fuera del alcance de la radiación solar. Los protectores solares deberían usarse en bebés mayores de 6 meses.
- Compruebe su piel de la cabeza a los pies una vez al mes.
Visite a su médico una vez al año para que le realice un reconocimiento profesional de piel. [Para aquellos que ya hayan tenido CCM, el seguimiento recomendado después del tratamiento es una vez al mes durante seis meses, una vez cada tres meses durante los próximos dos años, y a partir de ahí cada seis meses.]
